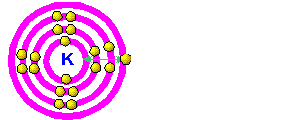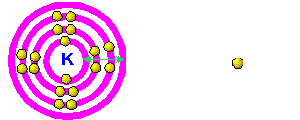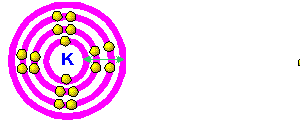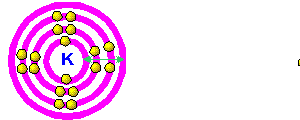

Kereaktifan Unsur-unsur Kumpulan I (Logam Alkali) |
|||
|
Apabila menurun ke bawah kumpulan I, saiz atom bertambah kerana bilangan petala bertambah. Elektron valens terletak semakin jauh daripada nukelus. Daya tarikan nukleus terhadap elektron valens semakin lemah. Elektron valens semakin mudah dibebaskan. Kesimpulan : Kereaktifan semakin bertambah apabila menurun ke bawah Kumpulan I. |
||